I. ĐỊNH NGHĨA, PHÂN LOẠI ANCOL
II. ĐỒNG PHÂN, DANH PHÁP
II. TÍNH CHẤT VẬT LÍ
IV. TÍNH CHẤT HOÁ HỌC
TÓM TẮT LÝ THUYẾT VỀ ANCOL
I. ĐỊNH NGHĨA, PHÂN LOẠI ANCOL
1. Định nghĩa
Ancol là những hợp chất hữu cơ vào phân tử có nhóm hiđroxyl -OH liên kết trực tiếp với nguyên tử cacbon no(1).
Bạn đang xem: Sơ đồ tư duy ancol
2. Phân loại
a) Ancol no, đơn chức, mạch hở
Phân tử bao gồm một đội -OH liên kết với gốc ankyl:Cn
H2n+1−OH
b) Ancol ko no, đơn chức, mạch hở
Phân tử có một nhóm -OH liên kết với nguyên tử cacbon no của gốc hiđrocacbon không no.
c) Ancol thơm, đơn chức
Phân tử gồm nhóm -OH liên kết với nguyên tử cacbon no thuộc mạch nhánh của vòng benzen.
d) Ancol vòng no, đơn chức
Phân tử gồm một team -OH liên kết với nguyên tử cacbon no thuộc gốc hiđrocacbon vòng no.
e) Ancol đa chức
Phân tử bao gồm hai tốt nhiều nhóm -OH ancol.
Xem thêm: Hướng dẫn cách sử dụng ssd hiệu quả, những kinh nghiệm khi dùng ổ cứng ssd
II. ĐỒNG PHÂN, DANH PHÁP
1. Đồng phân
Các ancol no, mạch hở, đơn chức có đồng phân mạch cacbon và đồng phân vị trí nhóm chức -OH (trong mạch cacbon).
2. Danh pháp
a) tên thông thường
Ancol + thương hiệu gốc ankyl + ic
b) Tên cụ thế
Tên hiđrocacbon tương ứng với mạch thiết yếu + số chỉ vị trí nhóm OH + ol
II. TÍNH CHẤT VẬT LÍ
Các ancol là chất lỏng hoặc chất rắn ở điều kiện thường. Nhiệt độ sôi, khối lượng riêng của những ancol tăng theo chiều tăng của phân tử khối ; ngược lại độ rã trong nước của bọn chúng lại giảm lúc phân tử khối tăng
Các ancol có nhiệt độ sôi cao hơn những hiđrocacbon gồm cùng phân tử khối hoặc đồng phân ete của nó là do giữa các phân tử ancol có liên kết hiđro(1).
IV. TÍNH CHẤT HOÁ HỌC
1. Phản ứng thế H của đội OH
a) Tính chất tầm thường của ancol
* Tác dụng với kim loại kiềm
Natri phản ứng với etanol giải phóng khí hiđro.
2C2H5−O−H+2Na→2C2H5−ONa+H2
b) Tính chất đặc trưng của glixerol
Thí nghiệm:
Cho vào nhị ống nghiệm, mỗi ống 3 - 4 giọt dung dịch
Cu
SO42% và 2 - 3 ml dung dịch Na
OH 10%, lắc nhẹ. Trong cả nhị ống nghiệm đều gồm kết tủa xanh của
Cu(OH)2:

Tiếp tục nhỏ vào ống thứ nhất 3 - 4 giọt etanol, vào ống thứ nhì 3 - 4 giọt glixerol. Lắc nhẹ cả nhì ống nghiệm. Vào ống (1): kết tủa không tan. Vào ống (2): kết tủa tung tạo thành dung dịch màu xanh lam của muối đồng(II) glixerat.
Sơ đồ bốn duy về Ancol by Đạt Phan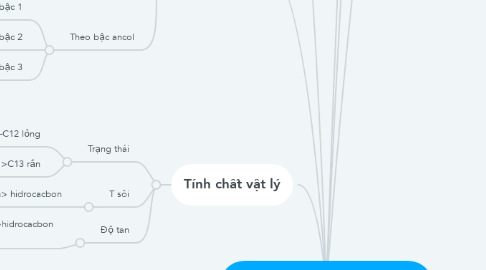
1. Định nghĩa
1.1. Là hợp chất hữu cơ links với đội OH
2. Phân loại
2.1. Theo cội hidrocacbon
2.1.1. Ancol no
2.1.2. Ancol ko no
2.1.3. Ancol thơm
2.2. Theo số lượng nhóm chức
2.2.1. Ancol 1-1 chức
2.2.2. Ancol đa chức
2.3. Theo bậc ancol
2.3.1. Ancol bậc 1
2.3.2. Ancol bậc 2
2.3.3. Ancol bậc 3
3. Danh pháp
3.1. Danh pháp thường
3.1.1. Ancol + cội hidrocacbon+ic
3.2. Danh pháp chũm thế
3.2.1. Stt-tên nhánh+tên mạch chính-stt-tên links bội-stt-ol
3.3. Danh pháp cacbiol
3.3.1. Gốc hidrocacbon+ cacbiol
4. Đồng phân
4.1. Đồng phân cấu tạo
4.1.1. Đồng phân mạch C
4.1.2. Đồng phân vị trí nhóm chức,vị trí nhánh
4.1.3. Đồng phân nhóm chức
4.2. Đồng phân quang, hình học
4.2.1. Hình học khi ancol ko no tất cả lk song hoặc vòng
4.2.2. Quang học khi gồm C bất đối
5. đặc điểm vật lý
5.1. Trạng thái
5.1.1. C1-C12 lỏng
5.1.2. >C13 rắn
5.2. T sôi
5.2.1. Ancol> dẫn xuất halogen> hidrocacbon
5.3. Độ tan
5.3.1. Ancol>dẫn xuất hidrocacbon>hidrocacbon (Do độ pcuc)
6. đặc điểm hóa học của monoancol
6.1. Làm phản ứng cắt lk O-H
6.1.1. Bội phản ứng cùng với KLK -> muối ancolat +H2 2R(OH)n +2n
Na -> 2R(ONa)n +n
H2
6.1.2. Công dụng với axit cơ học -> este
6.1.2.1. +H RCOOH +R'OH RCOOR' H2O
6.1.2.2. +H R(COOH)n +n
R'OH R(COOR')n +n
H2O
6.1.2.3. +H n
RCOOH +R'(OH)n (RCOO)n
R' +n
H2O
6.1.3. Phứng tạo ra ete cùng với dẫn xuất hal
6.1.3.1. ROH + R'X. ROR' +Na
X
6.2. Phứng giảm lk C-OH
6.2.1. Phứng với axit đậm đặc
6.2.1.1. ROH+HARA +H2O
6.2.2. Phứng cùng với PCl5, PBr3, PI3, SOCl2
6.2.2.1. ROH+PCl5 —> R-Cl + PCl3 + HCl
6.2.2.2. ROH+PBr3—> RBr +H3PO4
6.3. Phứng tách nước ( đề hidrat hóa)
6.3.1. Nội phân tử
6.3.1.1. >C-C >C=C ROR' +H2O
6.4. Oxi hóa
6.4.1. Hoàn toàn
6.4.1.1. Cn
H2n+2-2a
Om + O2 —> CO2 + H2O
6.4.2. Không hoàn toàn
6.4.2.1. RCH2OH + O2 —> RCHO +H2O RCHO +KMNO4/H2SO4 -> RCOOH
6.5. Phứng cùng với X2
6.5.1. X2+ Na
OH -> Na
OX +Na
X
7. Ứng dụng
7.1. Metanol
7.1.1. Chế tạo fomadehit, dung môi, cung ứng MTBE (metyl tert-butyl ete)
7.2. Etanol
7.2.1. Điều chế đietyl ete , axit axetic, butadien (sx cao su thiên nhiên buna)...
7.2.2. Dung môi hữu cơ
7.2.3. Đồ uống
8. Điều chế
8.1. Cn
H2n+ H2O ->HCn
H2n+1OH
8.2. 3Cn
H2n+ 2KMn
O4+ 4H2O ->3Cn
H2n(OH)2+ 2Mn
O2+ 2KOH
8.3. RXn+ n
Na
OH ->R(OH)n+ n
Na
X
8.4. R(CHO)n+ n
H2 ->,Ni
R(CH2OH)n
8.5. R-CO-R’ + H2-->,Ni
R –CH(OH) –R’
9. Tính chất của poliancol
9.1. Phản ứng với KLK -> muối ancolat +H2 2R(OH)n +2n
Na -> 2R(ONa)n +n
H2
9.2. Phứng với axit
9.2.1. Cơ học VD: etilen glicol +axit —> monoeste hoặc đieste
9.2.2. Vô cơ VD: R(OH)n +HX -> RXn +H2O
9.3. Bóc H2O
9.3.1. HO-CH2-CH2-OH + H+->HO-CH2-CH2-+OH2 HO-CH2-CH2-+OH2->HO-CH2-CH2++H2O HO-CH2-CH2+->HO-CH=CH2+ H+ HO-CH=CH2->CH3-CH=O
9.4. Phứng oxi hóa
9.5. Phứng đặc thù của poliancol có ít nhất 2 đội OH liên kề
9.5.1. Cu(OH)2








